Tras terminar una cirugía para corregir una malformación genética en el corazón de un recién nacido, el cirujano cardíaco pediátrico William DeCampli, del Hospital Infantil Arnold Palmer, en Florida, tenía una inquietud; no con la salud del menor, ya que la operación había resultado exitosa, sino con una de las tecnologías empleadas en ese tipo de intervenciones.
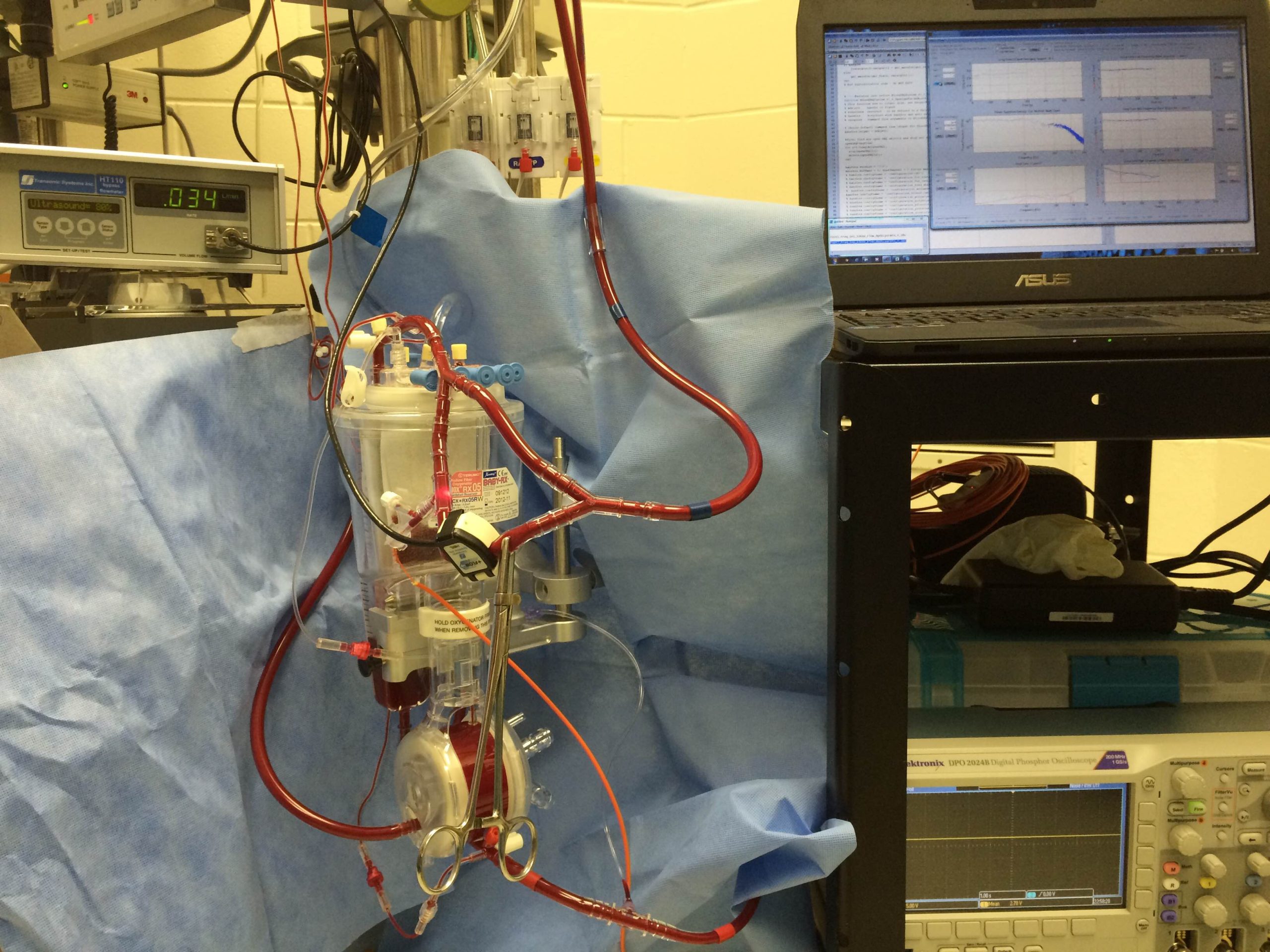
Como ocurre habitualmente en ese tipo de operaciones, el quirófano reunió a cirujanos, enfermeras, anestesiólogos y técnicos perfusionistas (operadores del equipo de bypass), pero aquel día había un par de personas más, dos investigadores especialistas en óptica y dinámica de fluidos complejos: Aristide Dogariu, de la Universidad de Florida Central y, quien en ese momento era su estudiante, José Rafael Guzmán Sepúlveda, actual investigador del Cinvestav Monterrey.
Su presencia tenía el objetivo de buscar una alternativa tecnológica para monitorear, prácticamente en tiempo real, el estado de coagulación de la sangre, ya que los equipos hasta ahora empleados como estándar de oro en los quirófanos (tiempo de coagulación activada y tromboelastografía) ofrecen resultados en no menos de 15 minutos, llegando a ser incluso cada 50 minutos, dificultando la labor del personal médico en tomar decisiones rápidas.
Las cirugías para corregir malformaciones cardiacas congénitas son realizadas, como se conoce en el argot médico, “a corazón abierto”.
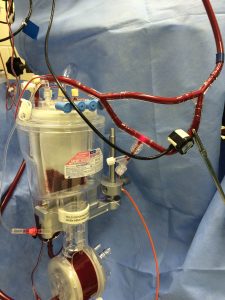
Estas delicadas intervenciones requieren la realización de una maniobra llamada bypass cardiopulmonar, donde son desconectados el corazón y los pulmones, al tiempo que la sangre es bombeada al resto del cuerpo por una máquina de circulación extracorpórea.
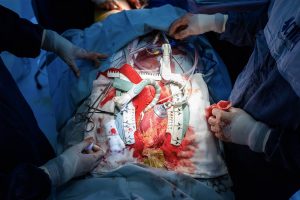
Ese proceso conlleva la fricción de este fluido corporal con la tubería de la máquina de circulación extracorpórea, pudiendo dar lugar a la formación de coágulos que ponen en riesgo la salud del paciente.
Pese a la administración de anticoagulantes durante la operación, es necesario monitorear el estado de coagulación de la sangre, ya que los químicos empleados para tal fin van perdiendo su efecto.
Al conocer ese problema, los investigadores sugirieron emplear un elemento ordinario como la luz, para determinar la coagulación de la sangre, utilizando un dispositivo basado en fibra óptica.
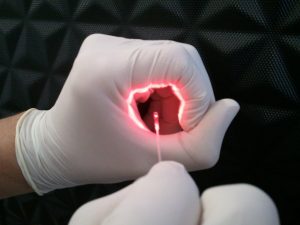
Esta alternativa representaba un cambio de paradigma, pues la tecnología propuesta mide la viscoelasticidad del plasma utilizando a los eritrocitos o glóbulos rojos como reporteros de su propio entorno.
A través de fibras ópticas se envía un haz de luz hacia la muestra de sangre y por esa misma vía es recogida la señal (similar a una señal de ruido), la cual se lleva a un detector (hardware externo) donde se determina la condición de la sangre.
“Al iluminar las partículas suspendidas de la sangre, el movimiento de los eritrocitos produce fluctuaciones aleatorias de la luz, mismas que pueden ser asociadas a las propiedades reológicas (comportamiento de deformación) del fluido donde se encuentran suspendidos; así es posible deducir si el ambiente de las partículas es normal o es más rígido, cuando empieza a tener lugar a la coagulación”.
“El principio del aparato es similar al de un interferómetro de camino común (donde las señales viajan por un mismo camino óptico), pero usamos fibra óptica para conducir un haz de luz de espectro ancho.
La punta de la fibra se introduce en el material a estudiar donde capta la información (luz esparcida) sin que sea susceptible de ruido o perturbaciones externas, como vibraciones mecánicas”, explicó el investigador del Cinvestav Monterrey.
El sensor fue patentado por la Universidad de Florida Central, pero al formar parte del proyecto, y tras ingresar como investigador al Cinvestav, Rafael Guzmán Sepúlveda siguió trabajando en la implementación de plataformas similares de sensado óptico basado en esparcimiento dinámico de luz, a partir de las cuales ahora ha podido abrir líneas de investigación sobre la composición de aerosoles, la dinámica de sistemas coloidales en ambientes altamente presurizados y, más recientemente, en ciencia básica sobre estudios de dinámica intracelular.
“En ese caso medimos el movimiento de los organelos dentro de las células de forma pasiva, sin contacto y sin marcadores fluorescentes. Este proceso es una mejora que abre muchas posibilidades para el uso de este sensor”, refirió Guzmán Sepúlveda.