La demencia es un síndrome de naturaleza crónica o progresiva que se caracteriza por el deterioro de la función cognitiva que afecta la memoria, pensamiento, orientación, compresión y el juicio, entre otras funciones; la más común es la enfermedad de Alzheimer, que representa hasta el 70 por ciento de casos de demencia a nivel mundial, reporta la OMS, y su estudio se torna difícil en modelos in vivo.
Con el propósito de entender mejor los procesos que dan origen a este padecimiento, Claudia Pérez Cruz, investigadora del Departamento de Farmacología del Cinvestav, se ha enfocado en describir los cambios que ocurren en el cerebro de la marmoseta común durante el envejecimiento.

El interés de estos estudios es encontrar un modelo de investigación más cercano al humano que permita analizar los mecanismos o factores de riesgo asociados con las demencias y eventualmente diseñar nuevos fármacos o tratamientos para poder prevenirlas.
Esta especie es un modelo de investigación atractivo, al ser un primate presenta una alta homología genética con el humano y un desarrollo cerebral más complejo que los modelos murinos (roedores); además, tiene una alta capacidad de reproducción, son de tamaño pequeño y muestran una vida media de 10 años, lo cual favorece el estudio del envejecimiento.
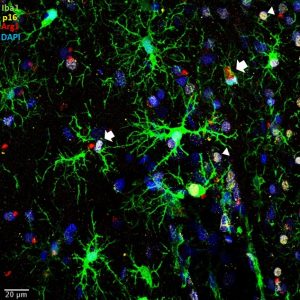
El grupo de investigación de Pérez Cruz observó que conforme la marmoseta envejece, aumentan los niveles de estrés oxidativo, hiperfosforilación de la proteína tau y microglía distrófica en el hipocampo, además de una notable presencia de placas amiloideas; en los animales más viejos, la microglía se torna disfuncional, perdiendo capacidad para almacenar hierro en su interior, metal que se acumula al interior de las células, y en el espacio extracelular.

Esta disfunción se ve relacionada con un mayor daño por estrés oxidativo inducido por hierro en las neuronas adyacentes, procesos comparables en el ser humano en el desarrollo de enfermedades neurodegenerativas.
Por otra parte, en las marmosetas adultas y viejas se observa una activación de los astrocitos, proceso relacionado con inflamación cerebral; sin embargo, en animales muy viejos los astrocitos ya mostraban daño celular (atrofia astrocítica) y neurodegeneración.
“Al explorar los cerebros de estos animales de diferentes edades, fue posible ver que los ejemplares más longevos presentaban características distintivas de procesos neurodegenerativos, que van más allá del envejecimiento, en especial, la acumulación de la proteína tau fosforilada en neuronas y células gliales, así como la distrofia microglial (células cerebrales o macrófagos encargados de limpiar el tejido), atrofia astroglial, y estrés oxidativo”, explicó la investigadora.
En el humano, durante el envejecimiento o en enfermedades neurodegenerativas, la microglía y los atrocitos pierden sus funciones, en roedores esta condición no se ha podido observar de manera espontánea porque solo viven hasta dos años, y este parece ser un evento relacionado con el envejecimiento; en cambio, la especie estudiada presenta una mayor longevidad llegando hasta los 20 años en cautiverio, y con esto se puede ver más ampliamente su proceso de deterioro cerebral.
 A pesar de que el envejecimiento es el principal factor de riesgo para desarrollar alzhéimer, esta especie de primate también presenta diversas alteraciones a lo largo de su vida relacionadas con una mayor probabilidad de desarrollar demencias en la vejez, como obesidad, diabetes e hipertensión.
A pesar de que el envejecimiento es el principal factor de riesgo para desarrollar alzhéimer, esta especie de primate también presenta diversas alteraciones a lo largo de su vida relacionadas con una mayor probabilidad de desarrollar demencias en la vejez, como obesidad, diabetes e hipertensión.
La marmoseta común al ser crecida en condiciones de cautiverio, no solo incrementa su esperanza de vida hasta los 20 años, sino que desarrolla alteraciones metabólicas (obesidad y diabetes) considerados factores de riesgo para padecer enfermedades neurodegenerativas.
Estos datos se presentaron en una revisión publicada en la revista Trends in Neuroscience que expone las características biológicas de este primate no humano y describe investigaciones que ha reportado el daño cognitivo y funcional durante su envejecimiento, además, discute los posibles factores asociados con la neurodegeneración.
La investigación tiene el interés de caracterizar a este primate no humano durante el envejecimiento, ya que a la fecha se ha reportado que no solo muestra signos de envejecimiento cerebral, sino que desarrolla varias características similares a la neurodegeneración en humanos; el objetivo final será poder evaluar la eficacia de fármacos contra las enfermedades neurodegenerativas.
“Estos nuevos modelos representan una estrategia para implementar la medicina traslacional por su gran cercanía filogenética con el humano y su mayor longevidad que ayudarán a entender las causas de la neurodegeneración”, sostuvo Claudia Pérez Cruz. Para consultar la información completa ver en: Cell Press. https://authors.elsevier.com/a/1gjmwbotq095r














